寻找每个细胞间的微小差异,单细胞技术为什么行


对于这项2009年才诞生的年轻技术,无论学界、企业界还是资本方都保持着充足的耐心与期待。
全文5109字,阅读约需10分钟
文|魏江翰
编辑|刘聪
来源|亿欧健谈
ID:EO-Healthcare
题图 | unsplash
世上没有两片完全相同的树叶,也没有两个完全相同的细胞。
细胞是人体功能的最基本单位。人类从一颗受精卵开始,逐渐演变成一个约120万亿个细胞的成人,这些细胞共享着同一套遗传信息,却在表达过程中产生了个体差异。正是这些或多或少的差异,影响着生物体的功能乃至健康。
科学家由此产生了一个疯狂的想法:想真正了解人体,也许可以从了解每一个细胞的差异开始。于是,以基因测序为切入点,人类拉开了单细胞研究的大幕。
目前,单细胞研究主要是为RNA测序 ,由于RNA(转录组)能决定基因表达情况而最终导致细胞差异,因此有着更为广阔的应用场景,包括研究肿瘤异质性,免疫细胞多样性,疾病发生机理,以及寻找新药物靶点等。
这项技术目前还主要服务于科研而非临床,但2015年后,相关论文集中在国际顶级学术期刊发表;10x Genomics 和BD Rhapsody等国际知名企业陆续成立。这一切事实都宣告单细胞测序已经初步克服了单细胞捕获通量受限这一核心瓶颈,完成了商业化落地。
未来,单细胞研究将朝临床方向迈进。多组学和空间位置信息等多层次信息证据整合的趋势已经成为共识。
虽然从国内情况来看,单细胞测序技术开发起步较晚,大部分公司还处于产品开发和早期市场验证阶段。但可以肯定的是,对于这项2009年才诞生的年轻技术,无论学界、企业界还是资本方都保持着充足的耐心与期待。

01
从更高分辨率解码生命
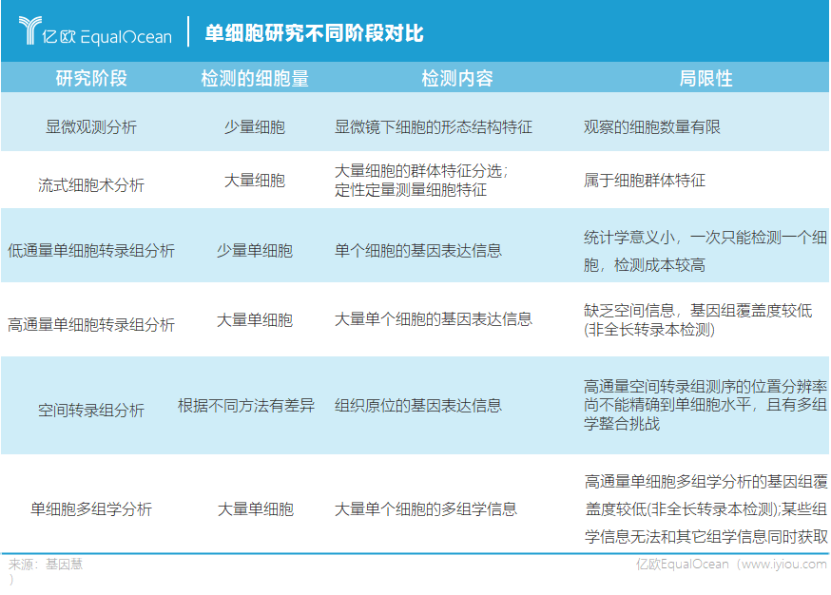
贝瑞基因单细胞业务科技服务部技术支持总监李哲对单细胞测序有着一个形象比喻:“组织测序像是一口吃掉一串葡萄,当中有酸有甜,但我们无从分辨,只能品尝到一个整体的、综合的口味,而单细胞则是一颗一颗品尝。”
在生物体上,如此聚焦在单细胞的基因测序可以帮我们找到每一颗“酸葡萄”,相当于从更高的分辨率解码生命。而这一想法最早被学界广泛关注是在2013年。
在整个基因测序领域,2013年都是一个重要的转折点。这一年,科学家们对早在十年前就宣布完成的人类基因组计划进行了打补丁和总结,发布了参考基因组序列GRCh38,被认为是当时的标准人类参考基因组。
科学家总是“贪婪的”,拿到基因图谱后,便顺理成章地开始了对基因表达进行分析,去界定已经解析的基因在人的所有细胞中将如何表达和变化。于是这一年,单细胞测序荣膺《自然-方法》的年度技术。
单细胞测序是相对于组织测序产生的概念。简单而言,就是通过NGS 技术检查来自单个细胞的序列信息来发现细胞差异,并更好地了解单细胞的功能。
这一畅想在2003年宣布人类基因组草图初步绘制完成时还是天方夜谭,因为单细胞测序技术2009年才横空出世,迈出这一步的是北京大学教授汤富酬。他在英国剑桥大学Gurdon研究所做博士后研究期间,发表了全球首个单细胞mRNA 建库测序方案,实现了单细胞水平的全基因表达测序。
这一研究成果在单细胞领域内树起了第一座里程碑,但缺点是细胞分离、捕获的成本十分高昂,由此带来的问题是只能检测少量细胞的单细胞基因表达、通量很低。因此该方案只能用于神经细胞、生殖细胞等稀有细胞的研究。
在流程方面,单细胞测序需要先将组织或体液中的细胞群分离成单个细胞,再对提取基因进行一定倍数扩增,使之达到现有测序深度的可及水平再展开测序,最终获取细胞异质性等关键信息。
事实上,比起测序本身,测序前处理才是单细胞测序的核心壁垒。人体细胞的平均直径只有10-20微米,如何从组织中解离和捕获这么小的细胞并形成规模效应,是从组织测序通往单细胞测序路上最大的拦路虎。
李哲解释:“早期我们需要用口吸管,在显微镜下把它吸出来,或者是激光显微切割技术,把细胞一个个地从组织上切下来,然后放到一个独立体系中做扩增、建库、测序。” 显然,李哲口中的这些方式需要极大的人力和金钱成本,而这一糟糕的情况在2015年才有了转机。

02
打破“低通量”桎梏
高通量的大门终于要被叩开了。
2015年,Steven A. McCarroll 等研究者在《细胞》上发表了基于微滴包裹单细胞和捕获磁珠技术的Drop-Seq方案,之后不久,Stephen P. A. Fodor等研究者也在《科学》上发表了基于微孔板分散、分隔单细胞及捕获磁珠技术的 Cyto-Seq 方案,同年问世的两种方案成为了开启高通量大门的钥匙。
“两把钥匙”对单细胞的 mRNA 建库进行了大幅成本优化,引发了行业极大反响,以至于两种方案公布后分别被迅速商业化,形成了当下全球范围内最头部的两家单细胞测序企业10x Genomics和BD Rhapsody。
李哲介绍,在2015年之前,传统单细胞测序的通量只有几十到上百个细胞。而如今的10x Genomics和BD Rhapsody等高通量单细胞平台能一次性实现成千上万的单细胞通量,一些情况下甚至能达到一次性捕获60到70万细胞的高通量水平。
Drop-Seq方案(微流控)和Cyto-Seq方案(微孔板)本质上核心逻辑一致:给每个细胞加上特有的标签序列,进行测序时把携带相同标签的序列视为来自同一个细胞,这样一次建库就可以测获单细胞的信息。
“简单来说,微流控可以简单理解为通过水管一滴一滴地滴水,将单细胞捕获到液滴中;而微孔板则类似把一群细胞从半空中抛下,它们会根据物理规律(泊松分布),分布到一些微孔当中。”诺禾致源单细胞业务负责人齐炜在采访中告诉亿欧大健康,两种方案间没有明显的优劣势,只是到达同一目的地的两种不同工具。
其实,无论微流控还是微孔板,希望达到的目的都是让单细胞成规模的形成独立反应体系,只不过前者利用液滴,后者利用了微孔。两种方案共同把单细胞测序送入了高通量时代。
高通量时代不仅是形容单细胞的捕获效率,也暗示着单细胞测序自身的高速发展。
2016、2017两年,10x Genomics和BD Rhapsody先后推出了自己的单细胞分析系,用于测序后端的数据分析。在2017 年 10 月,国际合作项目“人类细胞图谱计划(Human Cell Atlas,HCA)”正式公布,全世界的研究者们希望同人类基因组计划一样能绘制一张细胞图谱,囊括人类所有细胞类型的基因表达特征。
这一国际重磅计划彻底点燃行业的热情。2018年,单细胞被《科学》期刊评为十大科学突破技术;仅一年后,单细胞又一次入选《自然》的生命科学领域年度技术。在齐炜的印象中,2018年“能明显感到(单细胞测序)起势”,到2019年,则已然“在圈子里成为了明星”。

03
空间转录组是下一波浪潮
单细胞技术在2019年的明星光环很大程度上归功于其在空间位置信息层面的技术突破。
齐炜介绍,单细胞测序通常无法获取单细胞的位置信息。“过去单细胞测序要把整个组织打碎成单个细胞的悬液再进行处理,这样就丢失了位置信息,人们无从得知被测序的细胞来自组织上的哪一位置。”
而在2019年10月,10x Genomics带着自己的创新Visium空间转录组测序解决方案成功在纳斯达克上市,超过50亿美金的市值使之毫无疑问地成为全球的单细胞领头羊。
Visium空间转录组测序解决方案将研究重心放到了空间解析的全转录组mRNA表达,不仅可从组织切片中获取细胞的转录组信息,还能进一步测获其转录本所在的位置信息。
在单细胞二度摘走《自然》的生命科学领域年度技术后,卡罗林斯卡学院生物学家 Sten Linnarsson曾如此点评:“一切都与空间有关。空间单细胞转录组学是单细胞的下一波浪潮,对于研究人类疾病的实验室特别有用,人类疾病通常始于单细胞并在空间上传播。”
从逻辑上简单解释,Visium的原理就是在为细胞加上特有标签序列时补上了位置信息。更准确说,是给每个相似细胞的区域加上了位置信息。
这一技术还有待改进。齐炜表示,目前单细胞空间转录组技术的精准度还有待提升。因为严格来说,Visium并没有真正达到单细胞的水平,而是几个细胞的精度。“如果这一壁垒被突破,那很可能是一个爆发级产品。”她说。
李哲认为,即便技术尚未成熟,但Visium的里程碑意义依然毋庸置疑,因为其指出了单细胞未来的发展方向。时至今日,单细胞从“单细胞转录组”到“到单细胞多组学”和“空间位置信息” 已经是一个明显趋势。
一个已经形成的共识是,揭示单细胞实际的功能状态,必须要整合所有层次的证据,而不仅仅停留在基因表达层面,当下“四处出击”的多组学技术即是出于这一认知的产物。而对于单细胞而言,回溯其位置信息则是多组学之外另一个极其重要的维度。
李哲认为,只有把细胞放回其原来所处的组织位置再研究才能得到最真实的结果,因为组织中细胞与细胞之间有着非常多的相互作用。例如肿瘤微环境,其中有肿瘤细胞,有健康机体细胞,有免疫细胞、基质,还有所有相关调控的成分。如果把细胞分出来与放到微环境当中去比较,看这些基因在相互作用时怎么发挥功能,二者间一定有差别。
“就像一个人单独坐在会议室中,你观察他,可能会觉得这个人好像不容易接近,但如果把他放回他自身的朋友圈中,就可能发现他在自然地跟所有人在愉快交谈,是完全不同的状态。” 李哲说。

04
以技术特点对接应用场景
在10x Genomics带着单细胞空间转录组Visium登陆纳斯达克的同时,单细胞测序在地球另一边的中国也一片生机盎然。
2019年,嗅觉敏锐的投资者已经开始在国内甄选标的。万乘基因、百奥智汇、新格元生物、寻因生物等国内最早一批单细胞高通量测序企业在当年陆续开始融资;之后持续升温,到2021年,一级市场已经交出了“11家企业,15笔融资事件”的成绩单,参与者不乏高瓴、红杉资本、礼来亚洲基金、IDG资本等明星投资机构。
高瓴对亿欧大健康表示,虽然单细胞生物经历了前几年的爆发,但在下游制药和临床应用领域,无论国内外都仍处于早期阶段。国内的单细胞企业头部公司还未显现,而后来者依然有入场机会。
资本总是拥抱创新。如前文所说,测序前的单细胞捕获是核心环节,虽然已经实现了高通量操作,但最主流的微流控技术和微孔板技术并非完美,学界对这一领域的创新其实也从未间断。
今年2月,美国Parse Biosciences刚刚完成超过4000万美元B轮融资,以寻求将其可实现超低成本单细胞建库的split-and-pool技术商业化;国内德运康瑞研发的Paired-seq技术能够突破Cyto-Seq方案的泊松分布限制,虽然只能实现中通量的单细胞建库,但在临床穿刺样本等细胞量较少的应用场景中具备潜在优势。
在高瓴看来,单细胞企业最重要的不仅是技术本身的创新性,更是不同企业能否凭借自身的技术特点找到最合适的应用场景,从而最大化技术创新的价值。
值得注意的是,一些单细胞技术在近两年因应对疫情得到了技术验证。一些企业将单细胞测序用于指导和加速药物发现,摆到了投资人的眼前。2020年3月,疫情刚刚在美国蔓延之际,礼来与单细胞测序公司AbCellera Biologics迅速达成协议,共同开发新冠病毒抗体。
AbCellera掌握单B细胞测序技术,负责从新冠康复患者血清样本中筛选出高活性的中和抗体。在收到第一批新冠康复者的血液样本后的一周内,AbCellera迅速筛查了500万以上个免疫细胞,来从中寻找那些帮助患者中和病毒的抗体细胞。而基于这一协作诞生的礼来新冠抗体联合疗法在2021年的销售额为22.39亿美元。国内方面,丹序生物也与百济神州有着同样的合作。
早前,拜耳和诺华领投的Immunitas也表示在利用单细胞组学数据来挖掘新的靶点,指导药物开发。不过作为相对较新的尝试,AbCellera和Immunitas证明了单细胞技术在有更多应用场景值得期待,但疫情已近三年,单细胞在临床检测上的“哑火”也侧面显示目前这一技术距离临床应用可能还有一段路要走。
高瓴认为,从长远角度来看,临床应用一定是正确的方向,但短期内将单细胞测序推广到临床应用确实难度较大。
究其原因,主要是目前病人单细胞组学的数据积累不够,还不足以在单细胞组学和疾病进展、适用疗法、预后情况等临床指标之间建立起清晰明确的对应关系。此外,现阶段单细胞测序技术对于样本的新鲜程度,细胞量也有着严格要求。
多技术、多学科的交叉应用是单细胞技术发展的底色,但也对入局者垒起了更高的壁垒。就目前而言,单细胞测序广阔的前景清晰可测,而稳定的竞争格局尚未形成。这一赛道正等待更多的入局者,来做“难而正确的事”。
本文由亿欧健谈授权亿欧发布,申请文章授权请联系原出处。