The Innovation | 猴痘病毒:为什么新发/再发病毒总能领先我们一步?

图1 猴痘病毒 (Credit: WHO)
“我们永远无法控制超出人类认知范畴的新发疾病”。(Margret Chan,世界卫生大会,2013 年)
COVID-19大流行两年多,很多人疲于应对新发病毒和防控措施,此时猴痘病毒在这些人群中出现了。这绝不是不作为的理由,而新冠病毒的全球性传播凸显了及时并有针对性的干预措施在应对突发公共卫生事件中的重要性。
新冠病毒和猴痘病毒截然不同——前者是新发的RNA病毒,后者是已在非洲流行了数十年的人畜共患病DNA病毒。然而,在全球爆发初期,我们对两者均知之甚少。
截至2022年6月中旬,全球已有超过2000例猴痘病例,这些病例均出现在既往非流行地区的新发人群中(图2),包括美洲、欧洲、东地中海和西太平洋地区(数据来源:https://www.who.int/emergencies/disease-outbreak-news/item/2022-DON392)。得益于新冠病毒大流行期间大幅增加的测序产能,多个国家快速公布了猴痘病毒的全基因组序列。令人惊讶的是,分子流行病学分析发现,在猴痘病毒首次被人发现以前,已经有相当长的一段时间,甚至可能长达数年的人际传播。
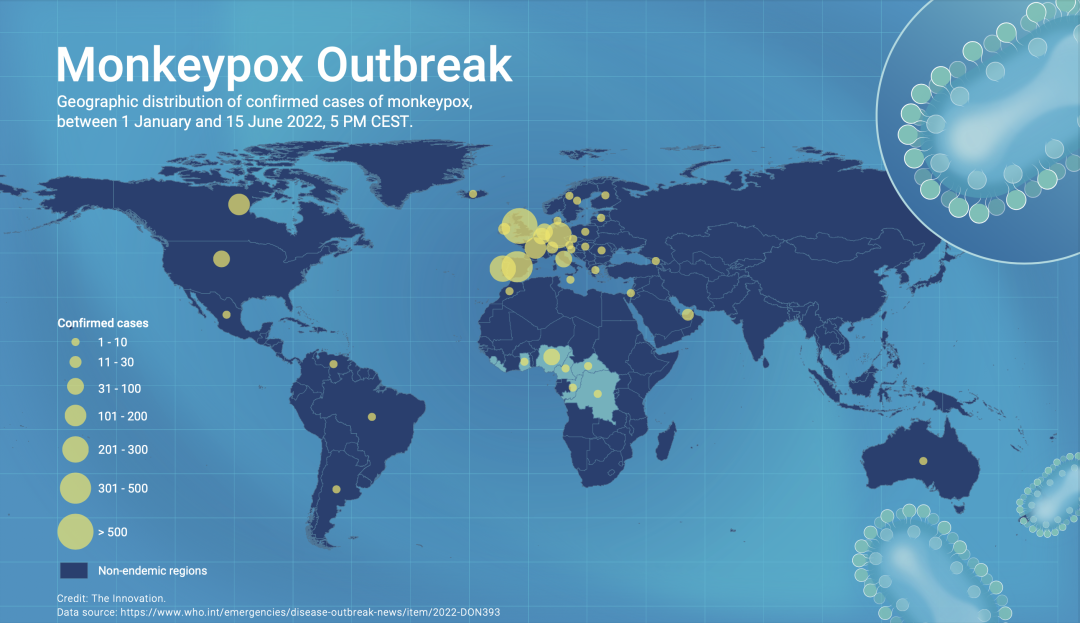
图2 图文摘要
与其他再发病毒一样,为什么这些熟知的病毒会突然出现?这不得不提醒我们,在搞清楚其传播动力学、病毒动力学、临床表现和愈后以前,不要乐观地认为再发猴痘病毒是轻微或易控的。考虑到目前尚无其基因组在人机体内如何演进的证据,且没有广泛可用的治疗手段和疫苗,因此,需要快速有力地行动来遏制病毒的传播。
1958年在进口的猕猴中,猴痘病毒首次被确定是脓疱疹相关轻度发烧的病因。与人类一样,猴子只是其偶然宿主。在该病流行的撒哈拉以南非洲地区,小型哺乳动物是其最有可能的宿主。尽管松鼠可能性最大,但确切的宿主仍然未知。因此,在猴痘病毒流行的国家,与啮齿动物的密切接触均具有感染风险。几十年来,中非和/或西非经常报告病例,这些病例由刚果和西非分支病毒造成,后者的毒性和传染性较低。
2022年之前,非洲以外地区很少出现确诊病例,且鲜有继发病例。在人群中,猴痘病毒通过直接接触体液或皮肤/黏膜损伤、被污染的物品(如被褥或衣物)或飞沫等途径进行传播。气溶胶传播的作用尚不明确,但其传播通常需要人与人之间的密切和长期接触。目前,在非洲以外地区出现的病例越来越多,传播链不明,但这些病例主要来自有多个性伴侣和/或有同性性行为的男性。正痘病毒的性传播途径已被认为适用于猴痘和痘苗病毒;然而,亲密关系中的密切接触与已知的传播模式是一致的。
对于埃博拉病毒和寨卡病毒,除人们熟知的性传播,其他诸多特征只有在大规模疫情爆发时才显现出来。60多年前,猴痘病毒已经被发现,但人们对其在血液、唾液、咽喉和溃疡中的病毒动力学却知之甚少,特别是在潜伏期和转阴后。在无症状病人中,尚不清楚猴痘病毒能否在精液中存在,或在精液中持续存在并导致性传播。对此,我们必须保持警惕。
基于流行病学特征判断,人类活动与当前猴痘爆发密不可分,这也带来了若干挑战。性传播并非猴痘的主要传播途径,因此高风险社区应该得到尊重。我们必须迅速识别和照顾受感染的患者,并采取严格的控制措施,在病毒进入普通人群和重症高风险人群(孕妇、免疫功能低下者和儿童)之前阻止传播。
猴痘患者的主要临床表现,在潜伏6-21天后,出现发烧等症状,仅有小部分感染者会出现水疱脓疱疹(图3)(首先在粘膜和面部,蔓延至全身直至手掌和足底)。目前,大多数病例以轻微和非典型皮疹开始,例如位于生殖器和/或肛周区域的孤立无痛溃疡性病变。因此,病例确诊必须迅速适应新数据,及时有效地传达给卫生保健机构、高危社区和普通人群;加强防疫宣传,早发现,早治疗。
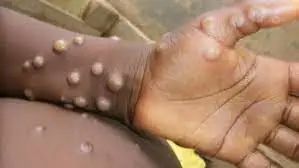
图3 猴痘病毒引发的疱疹 (Credit: WHO)
目前尚未收到人员伤亡报告,但估计致死率在1%—3.3%之间,因此不能被视为轻度疾病。在猴痘流行地区,4岁以下儿童的致死率甚至高达14%,且猴痘会导致孕妇流产。尽管猴痘在大多数流行国家可能未被充分诊断,在医疗资源匮乏地区,这些数字令人担忧。临床医生、公共卫生专家和病毒学家应及早行动起来,不能任由猴痘在地理上扩展,建立新的宿主,在人类之间持续传播。
天花和猴痘同属痘病毒科。天花是第一个也是唯一一个被消灭的人类病毒。与广泛感染哺乳动物的猴痘相比,天花仅限于人类。这使得通过疫苗接种得以根除——但它花了大约200年的时间、艰苦的国际努力最终在1980年得以根除。之后,疫苗接种被停止,导致40-50岁以下的人没有交叉保护性天花疫苗衍生的免疫力。此外,已经有几十年历史的天花疫苗的免疫力在接种疫苗的人群中正逐渐减弱。这个空缺的生态位,给了猴痘病毒机会。猴痘已在许多小型哺乳动物和灵长类动物中发现。虽然尚未在常见宠物中出现报告病例,但猴痘病毒完整的宿主范围,特别是在新的地理环境中尚不清楚。因此,在公共卫生实践中必须制定防止人畜传播的预防措施。由于痘病毒相对稳定,因此应加强对环境污染的监测,例如废水、家庭或医疗废物。
尽管痘病毒作为DNA病毒,其进化速度低于新冠病毒等RNA病毒,但其基因组具有很高的可塑性以快速适应新环境。对于猴痘病毒,研究表明每年每个位点大约105-106个突变频率,相当于每个基因组每年1-2个突变。2022年猴痘流行菌株基因组序列的初步结果表明,序列属于同一个进化枝,但与同源的2018年序列相比存在约40个突变位点的差异。以前,很少有来自非洲的序列,很明显这不足以代表其基因组的多样性。目前很难评估这些突变对临床诊疗或公共卫生政策制定的影响。
虽然一些卫生监管机构建议将Tecovirimat用于治疗猴痘患者,但现有的疗效证据很少,主要来自体外实验或动物实验。国际上已经加快开展临床试验,以确认其安全性和有效性。新冠大流行为猴痘病毒国际合作研究奠定了基础。考虑到疫苗和治疗方法在部分国家甚至全球范围内的可用性非常有限,因此,在仍有机会控制疫情的情况下,我们必须迅速采取行动。“殷鉴不远”应该作为各国卫生部门的指导宗旨。
总结与展望
猴痘病毒的复燃,伴随欧洲和北美努力控制该疾病的传播,人们不应忘记,这是在更大规模上消除非洲猴痘病毒负担的机会和责任。下一步的重点将是注重传染病的预防而不是应对。埃博拉病毒卷土重来、脊髓灰质炎死灰复燃、猴痘病毒再发,为人类敲响警钟!
责任编辑
张永龙 上海交通大学医学院附属第六人民医院
赵 琦 山东大学

扫二维码|查看原文
原文链接:https://www.cell.com/the-innovation/fulltext/S2666-6758(22)00069-8
本文内容来自Cell Press合作期刊The Innovation第三卷第四期以Editorial发表的“Different virus, same mistakes: why (re-) emerging viruses are one step ahead of us” (投稿: 2021-06-08;接收: 2022-06-11;在线刊出: 2022-06-22)。
DOI: https://doi.org/10.1016/j.xinn.2022.100273
引用格式:Vetter P., Jacquerioz F., Eckerle I. (2022). Different virus, same mistakes: why (re-) emerging viruses are one step ahead of us. The Innovation. 3(4),100273.
作者简介
Isabella Eckerle, Virologists, MD, Professor for Emerging Viral Diseases, University Hospitals of Geneva and University of Geneva. Study of medicine in Heidelberg, clinical work at the University Hospital Heidelberg, Research group leader Institute of Virology, University of Bonn Medical Centre, Research focus on emerging viruses and coronaviruses. High-level European Expert group proposing a roadmap towards stabilization of the Covid-19 pandemic in the European region, WHO Euro, World Health Organization and several other expert panels on COVID-19 and pandemic viruses, interests in pandemic prevention, diagnostics for emerging viruses, research at the One Health Interface.
往期精品(点击图片直达文字对应教程)
后台回复“生信宝典福利第一波”或点击阅读原文获取教程合集