猪器官移植再传捷报!全球首例猪肾脏成功移植入人体
排版:李雪薇
据悉,这是自 1992 年以来异种移植临床被紧急叫停后近30年以来,首例在人体中进行的异种移植研究。当年,美国匹斯堡大学进行了两例狒狒肝脏移植,患者分别活了 70 天和 26 天,另外有一名洛杉矶女性尝试了猪肝脏移植,但术后 34 小时就死亡了。
虽然纽约大学朗格尼医学中心移植外科 Montgomery 教授团队宣布手术成功,移植后猪肾脏没有出现排斥反应,且正常工作了 54 个小时,但是,这项具有重大意义的手术相关研究数据并未发表在同行评审杂志上,人们对此了解依据有限。
近日,阿拉巴马大学伯明翰分校 Heersink 医学院移植外科教授 Jayme Locke博士带领的研究团队同样完成了一例猪肾脏移植术,将经过基因编辑的猪肾脏移植到了一例 57 岁脑死亡男性体内,并发布了首个经过同行评审的猪肾脏移植论文,公布了异种肾脏移植的更多细节。

缓慢进展的异种器官移植
然而,仅在美国,就有 80 万人患有肾衰竭,超过 9 万人急需肾脏移植,但是每年仅有2.5万例患者得到了合适的肾源完成了手术,剩下大部分患者最终因病情恶化而去世。
由于许多动物跟人体的器官具有一定的相似性,且动物来源器官非常容易获得,因此,长期以来许多专家试图通过异种器官移植来解决器官短缺的难题,但这一过程并不顺利。
1963 年-1964 年期间,杜兰大学外科医生曾尝试将黑猩猩的肾脏移植到 13 例终末期肾病患者体内。由于当时肾透析技术还不成熟,这些患者必死无疑。然而,即使黑猩猩与人类之间有着密切的联系,但那些接受肾脏移植的人几乎都在数周内死亡。
但人们并没有放弃异种器官移植的梦想,毕竟 1954 年,同卵双胞胎之间的肾脏移植让患者的寿命延长了 8 年,这一“诱惑”让众多外科医生无法拒绝。
 (来源:Pixabay)
(来源:Pixabay)时间来到了 2000 年代,许多研究人员开始努力通过基因编辑技术来减少异种抑制排斥的发生。
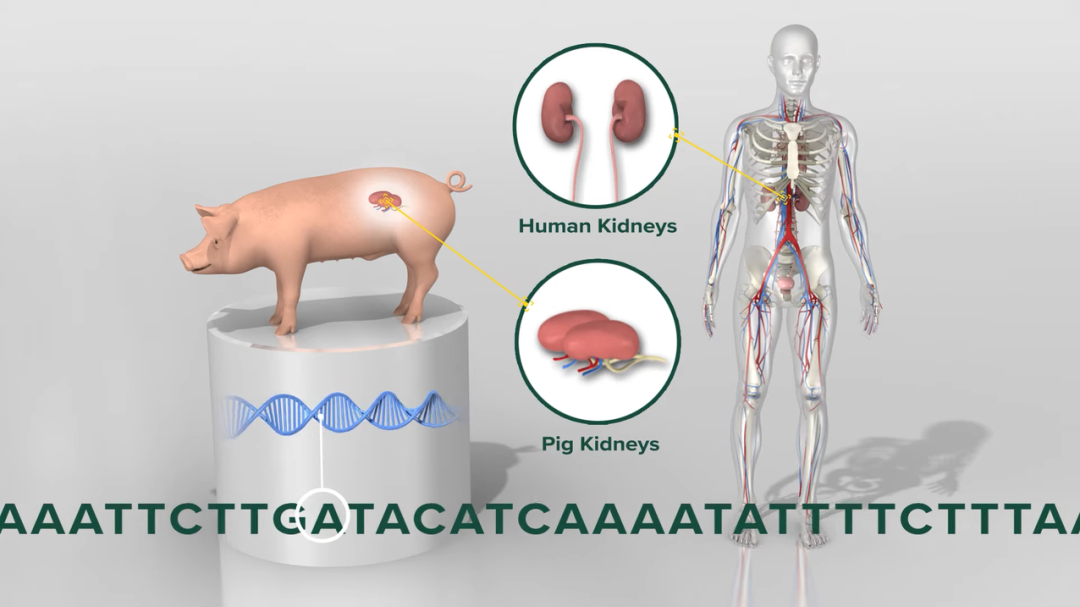
Revivcor 是一家专门提供转基因猪的生物公司,该公司旗下名为 Ukidney 的猪被专门用作异种肾脏移植供体来源。该供体猪共有 10 个基因发生了变化,其中猪体内的 GGTA1、β4GalNT2 和 CMAH 三个基因会引发急性排斥反应,因而被敲除。同样地,猪激素生长受体基因也被敲除,防止肾脏在受体体内生长。
 图 | 需要敲出和插入的基因(来源:UAB)
图 | 需要敲出和插入的基因(来源:UAB)基因编辑技术的进步,让人类离异种器官移植更近了一步。
首个异种肾脏移植手术细节公布
例如,猪的肾脏能否耐受成人体内的工作环境?要知道,非灵长类动物以及猪的动脉血压相比成年人明显降低,因此移植到人体后相当于长期在高血压的状态下工作。同样地,异种肾脏移植后再灌注时的血流动力学稳定性数据也非常重要,这能够反应异种移植物中的炎症介质清除是否会引发心血管衰竭。此外,手术过程是否会出现危机生命的并发症也需要仔细探究。
为此,研究人员首先从无菌养殖的洁净供体猪内取出肾脏,然后按照人类肾脏供体的储存、运输和加工方式进行处理以供植入。
随后,在手术前,研究人员对脑死亡受体和供体动物之间进行了交叉配型兼容性测试,以确定转基因猪肾脏及预期受体之间能能够良好的匹配。虽然,肾脏移植时人与人之间的交叉配型已经成熟,但是猪与人的组织匹配测试是研究小组单独开发的,并在这次试验中得到了验证。
最后,研究人员家那个供体猪的肾脏放置在人类受体肾脏解剖位置,将其与肾动脉、肾静脉以及其他附件连接起来,并给脑死亡患者使用标准的免疫抑制疗法。
不过,在试验过程中研究人员发现,只有一个肾脏正常产生尿液,另外一个肾脏并没有尿液产生。同时,产生尿液的肾脏也没有执行正常的肾脏功能,帮助清除血液肌酐。目前,研究人员尚不清楚为何两个肾脏之间尿量存在差异,也不清楚为何正常产生尿液的肾脏无法清除肌酐。
此外,病理专家在对肾脏进行活检监测的过程中发现,移植后的肾脏中有众多不明原因的微小血栓形成,研究团队也正在进行对此进行调查。
这些研究细节的公布意味着,异种移植并不像大众所期待的那样已经可以应用于临床,实际上它依旧充满了许多未知。未来,还需要更多的临床研究来解决异种移植所引发的一系列问题,从而真正造福人类。
据 Jayme Locke 博士表示,“利用脑死亡模型进行临床试验依旧存在很多局限,例如无法测量肾脏的基本功能。下一步,我们将进行I期临床试验,将猪的肾脏真正移植到活人体内,在更有利于肾脏恢复的环境下,检查异种肾脏移植的可行性。”
https://onlinelibrary.wiley.com/doi/10.1111/ajt.16930
https://www.uab.edu/news/campus/item/12566-uab-announces-first-clinical-grade-transplant-of-gene-edited-pig-kidneys-into-brain-dead-human

评论
